カロリー制限はなぜ老化を遅らせるのか
カロリー制限(calorie restriction)とは、摂取する食物のカロリーを削減することである。カロリー制限は、栄養失調をきたさない限り、様々な生物で老化の防止、加齢性疾患の減少、寿命の延長をもたらすことが確認されている。ダイエット目的で行われることもあるが、この言葉は、主として抗老化医学の分野で用いられる。本稿では、カロリー制限はなぜ老化を遅らせ、寿命を延ばすのか、カロリー制限にはメリット以外にデメリットもないのかについて考えてみたい。

二十世紀以前におけるカロリー制限の実践
カロリー制限の歴史は古い。紀元1000年頃に、ペルシャの哲学者で医者のイブン・スィーナー(アウィケンナ)は、中年以降の患者に、若い時よりも食事の量を減らすよう指導していたと伝わっている[1]。寿命延長方法としてのカロリー制限を公刊された著作で最初に提案したのは、ルネサンス期のイタリア貴族、ルイジ・コルナロ(Luigi Cornaro; 1484–1566年)である。コルナロは、若い時の不摂生がたたって病気になったが、医師の勧めで少食を実行したところ、一年足らずで快癒した。それ以来、彼は毎日食べ物を350グラムに限定したが、パン、パナド、卵、スープ、鶏肉、子羊、魚など多様な食材で栄養のバランスを取ったおかげで、健康を維持したまま、介護も不要な状態で長生きしたと伝えられている。

彼は自分の長生きを誇張し、年齢詐称を繰り返したため、102歳まで生きたということになっているが、実際は82歳ぐらいで亡くなったようだ[3]。それでも、当時の平均寿命を基準に考えるなら、十分長生きで、自分の食餌療法をまとめた『無病法』(原題:Discorsi della vita sobria 節制生活講話[4])は幅広く読まれて、食養のバイブルとなった。
日本でも、84歳まで生きた貝原益軒(かいばら えきけん, 1630 – 1714年)が『養生訓』で、「珍美の食に対すとも、八九分にてやむべし[5]」と、今日の「腹八分目に医者要らず」という諺に通じることを述べている。インドの伝統医学であるアーユルヴェーダにも似たような格言があり、小食が健康に良いことは、洋の東西で経験的に認識されている。しかし、カロリー制限によって様々な種の生物が寿命を延長させることが科学的に実証されるようになったのは、二十世紀になってからのことである。
動物実験によるカロリー制限の効果の検証
栄養失調のないカロリー制限が老化を遅らせ、寿命を延ばすことは、酵母[6]、ハエ[7]、クモ[8]、
魚[9]、齧歯類[10]など多くの種の生物において確認されている。もっとも、カロリー制限が免疫機能を低下させることもわかっており[11]、実験で寿命が延びたのは、ウイルスや菌が少ない人工的な環境であったからに過ぎないのではないかという懐疑論もある。そんな中、抗老化医学が最も注目する動物実験は、米国でウィスコンシン大学(the University of Wisconsin Madison=UW)と国立老化研究所(the National Institute on Aging=NIA)が行っているアカゲザル(Macaca mulatta, rhesus monkeys)に対する実験である。
アカゲザルは、アジアの広い地域に絶滅の恐れがないほど多く生息する旧世界ザルで、ヒトと遺伝子が93%同じであることから、人体実験の代替として使うことが適切な実験動物である。また飼育されているとはいえ、比較的自然環境に近い状態で飼われているだけに、免疫機能低下以上のメリットがあるかどうかも注目されるところである。
ウィスコンシン大学は、1989年から始めた実験の結果として、2009年に『サイエンス』で、カロリー制限がアカゲザルの寿命を延ばしたと報告した[12]。自由摂取の対照群と比べ、摂取カロリーを30%減らした実験群では、糖尿病、癌、心臓血管疾患、脳萎縮といった加齢関連疾患の発生率が減り、対照群の生存率が50%の時点で、生存率が80%であったというのである。以下の写真の左側は自由摂取をしたアカゲザル、右側はカロリー制限をしたアカゲザルが平均寿命に相当する高齢に達した時の写真で、右側のアカゲザルの方が左側よりも毛がふさふさして若々しいことがわかる。

これに対して、1987年から同様の研究を実施していた国立老化研究所は、2012年に『ネイチャー』で、カロリー制限がアカゲザルの寿命を延ばさないという逆の結果を報告した[13]。国立老化研究所は、ウィスコンシン大学よりも幅広い年齢のアカゲザルを集めて様々な年齢でカロリー制限を開始したが、どの年齢から始めた場合でも、カロリー制限を行った実験群は、中性脂肪やコレステロールの値が有意に低いなど、対照群と比べて代謝機能の改善が見られたものの、T細胞の増殖能が低下するなど、免疫機能の低下がそれを相殺して、生存率を高めなかったと分析している。
ウィスコンシン大学と国立老化研究所とで結果が逆になったのは、餌の量と質に違いがあるからと考えられている。ウィスコンシン大学の実験では、国立老化研究所の実験と比べて、餌に六倍の糖質、二倍の脂質が含まれていたが、後者では代わりに他の多様な栄養素がバランスよく含まれていた。また、ウィスコンシン大学の対照群では、アカゲザルがいつでも好きなだけ餌を食べられたのに対して、国立老化研究所の対照群では、食事が一日二回に限定されており、ウィスコンシン大学の対照群と比べると緩やかなカロリー制限を行っていたと評せられる。そこで、以下のような理由から「カロリー制限しても寿命は延びない」という懐疑論が出てきた。
カロリー制限により餌の量を自由摂取群の20~30%ぐらい減らしたとしても、それは、本来健康を維持するための適正量に近づいただけかも知れません。これまでのカロリー制限の実験では、過食による早死を防いだため、結果的に平均寿命や最長寿命が延びたように見えていただけなのかも知れません。[14]
確かに、カロリー制限にはメタボリック・シンドローム(通称、メタボ)を防止するという健康効果があるが、はたしてそれ以上の健康効果はないのか。この論争に決着をつけるべく、アラバマ大学の統計学者たちが2015年7月現在の両実験データを解析し、その結果を2017年に『ネイチャー・コミュニケーションズ』にて発表した。それによれば、以下のグラフに示されているとおり、左側のウィスコンシン大学(UW)でも、右側の国立老化研究所(NIA)でも、カロリー制限を受けた実験群(赤線)の方が、そうではない対照群(青線)よりも加齢関連疾患を持たない割合が高い傾向にある。

問題は、これが寿命延長につながっているかどうかである。研究チームはこの点を確認するために、各地で飼育している霊長類の寿命データベース(iPAD=the internet Primate Aging Database)を活用し、両施設での実験群と対照群で使っているアカゲザルの属性を平均と比較した。以下のグラフは、両施設のアカゲザルの体重を同じ年齢層のiPAD登録アカゲザルの平均と比較したもので、これを見ると、ウィスコンシン大学の対照群以外は、平均とほぼ同じ、もしくはそれ以下であることがわかる。このことは、老化研究所の対照群のアカゲザルも、穏やかなカロリー制限をした状態に近いことを示している。
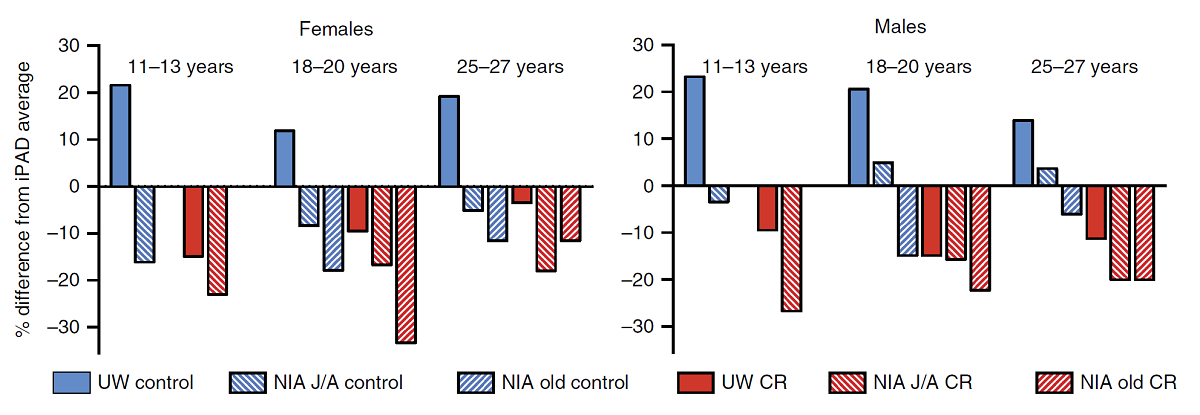
このグラフで特に注目したいのは、国立老化研究所で老年からカロリー制限を開始した実験群とそれに対応する対照群のオス、つまり右側の左下がりの斜線が入った棒グラフである。実験群のみならず、対照群も摂取カロリーが比較的少なく、その結果、体重も iPAD 登録アカゲザルの平均よりも小さい。そしてこれらのオスたちは、平均的なオスよりも長生きをしている。これらのオス20匹の寿命の中央値は、アカゲザルのオスの90パーセントタイル値である35歳で、6匹は40歳を超えて生存し、カロリー制限をしたオスの1匹は論文執筆時現在43歳で、過去最長記録を更新した。ここから、研究チームは、オスが老年になってから始めるカロリー制限には寿命延長効果があると結論付けた。
これに対して、若年/中年からカロリー制限を始めたオスには、寿命延長効果が見られなかった。これは齧歯類に対するカロリー制限実験の結果とは対照的である。齧歯類では、カロリー制限を始める時期が早いほど寿命延長効果が大きい。以下の表は、カロリー制限を受けた齧歯類の寿命延長効果を、寿命78歳のヒトに当てはめて試算したものである。例えば、1行目は、人生の20パーセントタイル値である15.6歳からカロリー制限を62.4年間行った場合、延長寿命は、15%のカロリー制限で5.6年、30%のカロリー制限で11.2年という意味である。最後の行は、人生の80パーセントタイル値である62.4歳からカロリー制限を15.6年間行った場合、延長寿命は期待できないということである。

これを真に受けて、若い時からカロリー制限に取り組んだ人もいるようだが、私たちは霊長類であるから、齧歯類の実験結果よりもアカゲザルの実験結果の方が参考になる。アカゲザルについても言えることだが、育ち盛りに行うカロリー制限は危険を伴う。メタボリック・シンドロームが発生するのは中高年になってからなので、カロリー制限もその時期から始めた方がよいということなのだろう。
他方でメスでは、カロリー制限による寿命延長効果は、開始時期とは無関係に認められなかった。同じことは齧歯類にも当てはまる[17]。メスが皮下脂肪を発達させるのに対して、オスは内臓脂肪を発達させる傾向があり、メタボリック・シンドロームの弊害はメスよりもオスにおいて顕著である。オスでは、カロリー制限が、寿命延長効果に加え、メタボリック・シンドロームの回避というメリットをもたらすのに対して、メスにはそうしたボーナスがなく、カロリー制限による寿命延長効果が免疫機能の低下というカロリー制限のデメリットによって相殺され、生存率の向上を帰結させなかったと考えられる。
人体に対するカロリー制限の影響の検証
カロリー制限がヒトの寿命を延ばすかどうかを検証するために、ヒトに対して、アカゲザルに対して行ったような実験を、被験者が死ぬまで長期にわたって十分コントロールされた状態で行うことは困難である。しかし、短期的にカロリー制限が人体にどのような影響を及ぼすかをランダム化比較試験で調べる前向き研究や長期間にわたって自発的にカロリー制限を実践している人をそうではない他の人と比べる後ろ向き研究なら可能である。
飢餓が人体に及ぼす影響を調べる前向き研究が、1944年から1945年の間に米国のミネソタ大学で行われたことがある。ただしこれは、カロリー制限が寿命を延長させるかどうかを調べようとした抗老化医学的実験としてではなくて、第二次世界大戦で飢餓に陥ったヨーロッパ人たちを救済するためのシミュレーションとして行った。被験者は兵役の代替として志願した22~33歳の白人男性で、当時のヨーロッパ人が飢えを凌ぐために食べていたジャガイモやパンやマカロニなどを一日あたり約1560キロカロリーに制限した半飢餓状態を24週間体験した。食事が炭水化物に偏っていたため、当然のことながら栄養失調の悪影響が被験者に出現した[18]。実験結果は『ヒトの飢餓の生物学』(The Biology of Human Starvation)として出版されたが、カロリー制限は必須栄養分を確保した上で、糖質など必須でない栄養分を減らすことが前提となるので、このミネソタ飢餓実験(The Minnesota Starvation Experiment)は、カロリー制限の人体実験としては扱われていない。
以下、カロリー制限と言えば、栄養失調のないカロリー制限(Calorie restriction without malnutrition)のこととしたい。この意味でのカロリー制限が人体に及ぼす影響を調べた前向き研究が、2007年から始まった。CALERIE(Comprehensive Assessment of Long term Effects of Reducing Intake of Energy エネルギー摂取削減の長期的効果の包括的評価)と名付けられたこのランダム化比較試験では、標準もしくは軽度の肥満(BMI=22-27.9kg/m2)で、20歳以上50歳以下の健康な男女228人のボランティアが募集された。ボランティアたちは、カロリー制限を実践する実験群と自由摂取の対照群にランダムに分けられ、実験群の82%と対照群の95%が24か月のプロトコルを完了した。被験者に重度の肥満者を含めなかったのは、カロリー制限が、肥満を解消することによる健康効果以上の寿命延長効果があるかどうかを調べるためである。
CALERIEの研究成果として以下のような発表がなされている。
- 2015年7月の発表[19]によると、実験群は 11.7±0.7% のカロリー制限を達成し、10.4±0.4% の体重減少を維持したのに対して、対照群の体重変化は無視できる程度であった。対照群と比べ、実験群において、トリヨードサイロニンとTNF-αが有意に減少した。トリヨードサイロニンは、細胞の代謝率を上昇させる甲状腺ホルモンの一種で、カロリー制限でこれが減少したのは、基礎代謝量が減ったからであると考えられる。TNF-αは、炎症を起こした細胞を壊死させ、感染を防ぐサイトカインで、TNF-αの減少が寿命を延長させることを示す確固たるエビデンスは存在しないが、こうした炎症指標値が加齢関連疾患の増加に伴って上昇することも事実である。
- 2015年9月の発表[20]によると、対照群と比較して、実験群では、骨形成の指標である骨型アルカリフォスファターゼ(bone-specific alkaline phosphatase)および健康寿命を維持する上で重要な部位(腰椎、大腿骨、大腿骨頚部)における骨密度(bone mineral density 骨塩量)が有意に低下した。カロリー制限を実践すると、身体活動が低くなり、そのために、骨が脆くなったということも考えられるが、それ以外にも要因はありそうだ。重回帰分析によれば、身体活動の変化以外にも、体の組成、ホルモン、栄養素の変化が、実験群における骨代謝と骨密度の変動の約31%を説明する。それゆえ、骨量減少が運動で予防できるかどうかはわからず、安全性に懸念が生じた[21]。
- 2016年7月の発表[22]によると、対照群と比較して、実験群では、炎症の指標である白血球総数、リンパ球数、C反応性蛋白、レプチン(食欲を抑制し、エネルギー消費を増加させる肥満ホルモンでもある炎症性サイトカイン)を二年後有意に減少させた[23]。白血球、その中でもリンパ球は、免疫機能を担う重要な細胞で、以下のグラフにあるとおりこれらが減ったにもかかわらず、実験群と対照群との間に過敏症の皮膚反応やワクチンに対する抗体応答に差がなく、カロリー制限が臨床的に重要な感染症を惹き起こすことはなかった。この結果から、研究者たちは、カロリー制限は、細胞性免疫を損なうことなく炎症を抑えると結論付けた。

以上を要するに、ヒトを対象にしたカロリー制限は、体重を減らすのみならず、白血球数、C反応性蛋白、TNF-α、レプチンといった炎症の指標となる値を減少させるので、抗炎症作用があり、それゆえ抗老化・寿命延長効果が期待できるということである。しかし、炎症を減らすことは、寿命を延ばすために望ましいことなのか。
炎症には比較的早期に収まる急性炎症と長期にわたって続く慢性炎症とがある。急性炎症は、白血球が体内に侵入してきた細菌やウイルスといった異物を攻撃する免疫の結果起きる場合が典型例で、炎症自体は好ましくないにしても、必要な自己防衛反応であるといえる。これに対して、慢性炎症は、アレルギー性疾患など自己防衛反応が暴走する結果、あるいは内的な生体異常の結果として起きると考えられ、さらには、加齢関連疾患と関係付けられている。それで、慢性炎症を防ぐことが寿命延長につながると研究者たちは予想しているのである。
CALERIEの研究者たちは、ヒトの場合、動物の場合とは異なり、カロリー制限が免疫機能を低下させることなく慢性炎症を防ぐと言うが、この実験だけでそう断定することはできない。死ぬまで行う動物実験とは異なり、CALERIEは、80歳近くまで生きるヒトに対してたった2年間しかカロリー制限の結果を追跡していない。しかも被験者は20歳以上50歳以下で、高齢者は含まれていない。更年期に当たる50歳以降、ヒトの免疫機能が低下することが知られており、それに伴って感染症による死亡が増える。カロリー制限で白血球などの免疫細胞を減らすことが高齢期にどのような影響を与えるかは、CALERIEの結果からはわからない。
もっと長期間カロリー制限を実践したときの影響を調べようとするなら、自発的にカロリー制限を長期間実践している人たちに対して後ろ向きに研究するしかない。幸い、そういう実践をしている集団がある。米国にある非営利組織、カロリー制限協会(The Calorie Restriction Society)はその代表で、1993年に Usenet 上にできた Sci.life-extension という名前のディスカッション・グループを前進として形成された国際的コミュニティである。2016年に、カロリー制限協会で3〜15年間カロリー制限を実践している37人の男女をその被験者たちと性と年齢を合致させた通常(西洋)食の摂取者および性と年齢と体脂肪率を合致させたマラソンランナーと比較した研究が発表された[24]。
それによると、カロリー制限実践者の骨格筋で測定した血清コルチゾール濃度は、通常食摂取者やマラソンランナーと比べて、高かった(それぞれ、15.6±4.6ng/dl、12.3±3.9ng/dl、11.2±2.7ng/dl; p≦0.001)。研究者たちは、それを炎症の減少、機能不全のタンパク質およびオルガネラの除去による細胞の品質管理強化と肯定的に評価している。この結果は、カロリー制限により血糖値が下がり、血糖値を高めるためにコルチゾールが分泌され、筋肉の分解と糖新生が促進されたからと考えられる。タンパク質の分解による新陳代謝の促進が炎症を減らしたことは肯定的に評価できるが、他方で、コルチゾール濃度の上昇は免疫機能を低下させ、不妊をもたらし、骨の形成を阻害するなどの副作用がある。2015年9月の発表で示された骨代謝と骨密度の低下もこれと関係がありそうだ。
そうした副作用のおかげでカロリー制限を途中でやめる人もいるはずだが、後ろ向き研究では脱落者が最初から除外されている。前向き研究のCALERIEでも、実験群では対照群以上の脱落者を出した。高齢になると免疫機能が低下するうえ、骨も脆くなってロコモティブ・シンドローム(骨、関節、筋肉など運動器の衰えが原因で健康寿命が短くなる運動器症候群)のリスクも高まる。それにもかかわらず、高齢になるまでカロリー制限を続けたとして、なおも寿命が延びるのかどうかに関して、これまで紹介した研究は説得力のある結論を出していない。被験者が死ぬまで実験を続けることが難しいのであるから、これは止むを得ないことだ。
カロリー制限の直接的な結果とみなすことはできないが、体重と死亡率の関係に関しては多くの調査があり、これがある程度参考になる。スウェーデンのヨーテボリ大学が、70歳の非喫煙者が15年間で死亡する割合を調べたところ、男性は、BMI=27-29kg/m2、女性は、BMI=25-27kg/m2で最も低く、70歳から75歳にかけて体重を10%減らすことは死亡率を有意に高めた[25]。BMIは、18.5以上25未満が標準とされている[26]ので、軽度の肥満の方が標準よりも長生きしたということである。中高年の日本人を対象にした研究でも、死亡リスクが最も低くなるBMIは、標準よりわずかに肥満気味の範囲(21-27kg/m2)であることが示された[27]。
50–71歳の非喫煙者を12.5年間フォローアップした米国の国立衛生研究所の研究[28]によれば、18歳から50歳の間における体重増加が死亡率を上昇させるのに対して、50歳から69歳の間における0.2–0.6kg/年程度の体重増加は死亡率を低下させ、体重減少は死亡率を上昇させる。体重減少が死亡率を高めたことに関しては、体重が減ったから病気になったのではなくて、病気になったから体重が減ったという逆の因果関係も考えられるが、50歳から69歳の間健康であった人でも、0.2–0.6kg/年の体重増加が死亡率を下げており、逆の因果関係だけでこの結果を説明することはできない。
BMIの研究における体重減少の原因はカロリー制限とは限らないので、直接的な証拠にはならないが、動物実験の結果と合わせて考えるなら、ヒトにおいても、カロリー制限には抗老化・寿命延長効果というメリットがある反面、免疫機能の低下というデメリットもあると言えそうである。次節では、このトレードオフはどういう分子レベルのメカニズムによって起きているのかについて考えてみたい。
トレードオフの分子生物学的機序
カロリー制限がなぜ老化を遅らせ、寿命を延長させるのかに関して、古くから様々な仮説が提案されてきた。代表的な仮説は、カロリー制限によって代謝速度を落とすと、代謝で発生して、老化を促進する活性酸素種のレベルを抑制するがゆえに、老化が遅滞するという生命活動速度理論に基づく仮説である。しかし、生命活動速度や活性酸素によって老化の速度を説明する理論自体が疑問視されているので、この仮説は支持できない。
解糖系での嫌気的代謝が亢進し、ミトコンドリアでの好気的代謝が低下すると細胞の老化が抑制されることからもわかるとおり、酸化ストレスは細胞の老化をもたらす。他方で、摂取カロリーを制限すると、解糖系での嫌気的代謝が低下し、ミトコンドリアでの好気的代謝を低下するにもかかわらず、個体の老化を抑制する。酸化ストレスが老化をもたらすと主張する近藤祥司は、細胞老化と個体老化は違うとしつつも、この矛盾は「現時点では、説明が非常に難しい問題[29]」と言っている。しかし、これに対する説明はそれほど難しくはない。細胞が老化しても、それを個体が新陳代謝する限り、個体は若さを維持できる。個体の老化は、酸化によるダメージによって直接起きるのではなくて、酸化によるダメージを修復する能力が衰退することで起きる。そして、カロリー制限はその能力を維持させると考えれば、説明がつく。
酸化ストレス老化説と並んで、もう一つ古くからある説として、ホルミシス(Hormesis 閾下増進効果)説がある。低線量の放射線など、本来有害なストレスも、微量ならかえって健康に良いという説である。確かに飢餓も度が過ぎれば死をもたらす有害なストレスであり、カロリー制限協会のメンバーは、ストレス・ホルモンであるコルチゾールの血清濃度が高いことは既に紹介した。とはいえ、ホルミシス説自体理論的裏付けがなく、この言葉を持ち出したところで何の説明にもなっていない。コルチゾールには、健康に有害な効果もあることは既に述べた。
現在支持を集めているのは、進化論的な、つまり自然淘汰による説明である。すなわち、カロリー制限による寿命延長メカニズムは、栄養が不十分な時期に親の寿命を延長させ、生殖を先延ばしにすることが子孫の確実な生存につながるがゆえに、幅広い種に備わるようになったというものである[30]。もっとも、この自然淘汰説だけでは、なぜカロリー制限が免疫機能や運動機能を低下させるのかがよくわからない。
カロリー制限の進化論的意義は、また後で考えることにして、ここでは、カロリー制限が寿命を延長する分子生物学的メカニズムについて考えたい。1999年に、レオナルド・ガレンテのグループは、酵母を用いた実験で、サーチュイン遺伝子(酵母の場合、Sir2)の活性化により、酵母の寿命が延びることを見出し[31]、2000年には、カロリー制限によって誘導される寿命の延長には、内呼吸の酸化剤であるNAD+が必要であることを示した[32]。
サーチュイン遺伝子が寿命を延ばすのは、その発現が、FoxO(Forkhead Box O フォークヘッド転写因子)を通じて、オートファジーを活性化することによってである[33]。オートファジーとは、自分の細胞の中で不要になったタンパク質などを分解して必要な栄養素を取り込むことで、栄養素が足りない事態への適切な対応である。体内のごみが一掃されることで、免疫システムが体内の異物を攻撃する必要が減り、その結果、慢性炎症を防ぐことになると考えられる。
カロリー制限がサーチュイン遺伝子(ヒトの場合、SIRT1)を活性化する一方で、この遺伝子は、増殖シグナルを伝達する酵素、mTOR(ヒトの場合、mTORC1)を阻害する[34]。mTORC1は、栄養が豊富にある場合、それを材料とエネルギー源として、細胞の数を増やす。カロリー制限の時とは逆に、オートファジーは抑制され、細胞にごみが溜まり、悪性腫瘍が発生しやすくなる。その代わり、それらを攻撃する免疫機能は強化される。
ヒトに対する実験で明らかになったカロリー制限による骨密度の低下はタンパク質不足が原因のようである。骨粗鬆症になりやすい閉経後女性を対象にした実験では、カロリー制限をしつつも、タンパク質が豊富な食事を食べた被験者は、タンパク質の量が通常であるカロリー制限実践者と比べて、インスリン様増殖因子1(IGF-1)が増加し、骨密度の低下が改善された[35]。IGF-1の増加は、PI3K/Aktシグナル伝達系を通して、mTORC1を活性化させ、SIRT1の発現を阻害する[36]。
どうやら、骨への悪影響を避けて、SIRT1活性化による寿命延長効果を得るという好いとこ取りはできないようだ。オートファジーによるタンパク質の分解が筋肉を衰えさせることを併せて考慮に入れるなら、栄養が足りない環境下では、無駄に体を動かしてエネルギーを浪費しないように、筋肉や骨といった運動器官の機能を低下させるという適応がなされていると考えられる。
シグナル伝達の結果をまとめると、カロリー制限は、オートファジーによる新陳代謝を促進して老化を防ぐ反面、免疫機能や運動機能を低下させる。カロリー制限をせずに十分な栄養を取ると、体が成長し、免疫機能も運動機能も向上する反面、老化の進展が速くなる。このように、カロリー制限には、「あちら立てれば、こちらが立たぬ」というトレードオフの関係がある。このトレードオフには、進化論的にどのような意義があるかについて、次節で考察することにしよう。
トレードオフに見られる二つの生存戦略
CALERIEの研究者たちは、カロリー制限の長所を強調するが、カロリー制限に長所しかないなら、なぜサーチュイン遺伝子は無条件で活性化されないのか。実際のところそうでないのは、個体が長生きすることは必ずしも種の利益にはならないからだ。もしも個体の長生きが種にとっても無条件に良いことであるなら、個体が不老不死になるように生命が進化したはずだが、そうならずに、逆に死が発明され、有性生殖が誕生し、個体が一定の寿命以上生きられないようにしたのは、その方が寄生者対策として有効であるからというのが今日の有力な仮説である。
カロリー制限による老化の遅延は、栄養が不十分な環境下で生殖を遅らせるという適応的な意味があると考えられている。拒食症の少女が無月経になって、思春期を遅らせる事実は古くから知られており、カロリー制限が妊娠を先送りするメカニズムは、着実に子孫を残す時期を選んで出産できるように適応したことで生まれたという説がある[37]。男に関しても、長期にわたるカロリー制限が、男性ホルモンであるテストステロンと結合する性ホルモン結合グロブリン(Sex Hormone–Binding Globulin=SHBG)の血中濃度を増やし、その結果、血中に遊離するテストステロンを減らし、生殖機能を低下させることがわかっている[38]。
マウスを用いたカロリー制限の実験[39]によると、離乳時に開始した場合はもちろん、成獣後に開始した場合でも、生殖の時期が遅滞する。自由摂取したメスのマウスが、15.5ヶ月齢で生殖能力が衰えるほど老化が進んだのに対して、4か月間カロリー制限をした後、15.5ヶ月齢で自由摂取したメスのマウスは、23ヶ月齢まで子を産んだ。自由摂取したマウスが10〜23ヶ月齢という高齢で出産した子が22%しか生存しなかったのに対して、カロリー制限後に自由摂取をしたマウスが15.5〜23ヶ月齢で娩出した子の73%以上は合併症なしに生き残った。通常、高齢出産はリスキーであるものだが、カロリー制限で老化を遅延させた場合はそうではないということである。
なお、2012年のメタアナリシス[40]によると、同系交配のマウスは、カロリー制限で寿命が逆に短くなる傾向がある。同系交配を続けると、マウスの遺伝的多様性が失われる。種の存続という観点からするなら、食料不足という危機を乗り越える上で、遺伝的多様性のない個体を多数生き残らせることは有利ではないから、この事実は、進化論的に見て合理的と言える。これに対して、遺伝的多様性のあるマウスには、他の動物と同様に、カロリー制限による寿命延長効果がある。
話を霊長類に戻そう。カロリー制限による寿命延長効果の意義が、出産の時期を餌が豊富になるまで先送りすることだとするなら、若い時ほど効果がある齧歯類とは違って、高齢になっても効果がある霊長類のカロリー制限の寿命延長効果はどう説明すればよいのだろうか。これは、霊長類が、齧歯類とは異なり、出産後長期にわたって子育てをすることで説明できそうだ。つまり、餌が不足する環境になると、たんに子供が発育を遅らせるだけでなく、未熟な子供を保護し、育てる親までが、老化を遅らせて長生きするようなメカニズムになっていると考えられる。
では、メスよりもオスでカロリー制限による寿命延長効果が出ることはどう説明するべきか。哺乳類では、メスは胎児を育てるエネルギーを確保するために、皮下脂肪を蓄えなければならない。だから、メスがある程度の皮下脂肪を蓄えても寿命が縮まることはない。これに対して、オスの仕事は戦うことであり、仕事をせずに内臓脂肪を貯め込む穀潰しのようなオスがメタボで早死にすることは種の利益に合致するがゆえに、こうした性差が生まれたと考えられる。しかし、メタボ回避による寿命延長は、カロリー制限による寿命延長とは区別しなければならない。
カロリー制限による寿命延長が運動機能や免疫機能の低下をもたらすのはなぜなのかに関しても合理的な説明が可能だ。食料が少ない環境では、運動しても無駄にエネルギーを消費するだけなので、それよりもオートファジーによって当面のエネルギーを確保する方が確実に生存できる。オートファジーが体内のごみを減らし、その結果、慢性炎症を防ぐ効果があることは既に述べた。内的異物が減っても、ウイルスや細菌など外的異物の侵入に対して免疫機能は依然として必要であるが、食料が少ない環境では、寄生者も少なくなるので、免疫機能の必要性も減る。
食料が豊富な環境で生きる場合と食料が乏しい環境で生きる場合の違いは、都会で生きる場合と田舎で生きる場合の違いに似ている。金を稼ぐなら田舎よりも都会である。都会は人口密度が高いし、金持ちもたくさん住んでいる。それだけに、詐欺や強盗などを行って、その富を掠め取ろうとする寄生者も多く、防犯のニーズが高い。これに対して、田舎は人もまばらで概して貧しいので、都会にいるような寄生者は少なく、それゆえ防犯意識も低い。
生命にとっての個体レベルでの防犯装置は免疫システムであるが、種レベルでは有性生殖である。特に、多様な個体をたくさん作り、一個体あたりの寿命を短くすれば、寄生者による乗っ取りのリスクを低減することができる。だから、十分な栄養摂取は、
IGF-1 → PI3K → Akt → mTORC1
というシグナル伝達系を通じて、免疫機能を強化しつつ、個体の成長と生殖を加速させ、寿命を短縮する。逆に、栄養が不十分になると、
NAD+ → SIRT1 → FoxO
というシグナル伝達系を通じて、免疫機能を弱めながらも、個体の成長と生殖を遅滞させ、寿命を延長させる。
このように、生命には、せわしい都会で太くて短い人生を送るか、それとものんびりした田舎で細くて長い人生を送るかという選択肢がある。この選択は、本来環境によって決まるものであり、個人が環境を無視して自由意思で決めるものではなかった。だから、寿命延長を目当てにカロリー制限をする前に、このメカニズムの意義を理解して、運動機能や免疫機能の低下に対する対策を別途取らなければならない。さもないと、防犯意識の低い田舎者が都会に来た時にありがちな憂き目に遭うことになるだろう。
参照情報
- ジェームズ・W・クレメント『スイッチ―オートファジーで手に入れる究極の健康長寿』日経BP (2021/1/8).
- デビッド・A・シンクレア『ライフスパン―老いなき世界』東洋経済新報社 (2020/9/16).
- 小林 武彦『寿命はなぜ決まっているのか 長生き遺伝子のヒミツ』岩波書店 (2016/2/19).
- 森望『寿命遺伝子 なぜ老いるのか 何が長寿を導くのか』講談社 (2021/3/18).
- 山田悟『カロリー制限の大罪』幻冬舎 (2017/6/21).
- 山本 雅, 仙波 憲太郎, 山梨 裕司『イラストで徹底理解する シグナル伝達キーワード事典』羊土社 (2012/8/7).
- ↑Schäfer, Daniel. “Aging, Longevity, and Diet: Historical Remarks on Calorie Intake Reduction.” Gerontology 51, no. 2 (2005): 126–30.
- ↑“Luigi Cornaro. Line engraving by F. Clerici.” Licensed under CC-BY-SA. Wellcome Library, London.
- ↑Giuseppe Gullino. “CORNER, Alvise".” Dizionario Biografico degli Italiani. Volume 29 (1983).
- ↑Discorsi della vita sobria del sig. Luigi Cornaro. Ne’ quali con l’essempio di se stesso dimostra con quai mezzi possa l’huomo conseruarsi sano infin’all’vltima vecchiezza. Giacomo Mascardi, 1616.
- ↑「珍美の食に対すとも、八九分にてやむべし。十分に飽き満るは後の禍あり。少しの間、欲をこらゆれば後の禍なし。少のみくひて味のよきをしれば、多くのみくひてあきみちたるに其楽同じく、且後の災なし。万のむくひて味のよきをしれば、多くのみくひて、あきみちたるに其楽同じく、且後の災なし。万に事十分にいたれば、必わざはひとなる。飲食尤満意をいむべし。又、初に慎めば必後の禍なし。」貝原益軒『養生訓』308.
- ↑Lin, Su-Ju, et al. “Calorie restriction extends yeast life span by lowering the level of NADH." Genes & development 18.1 (2004): 12-16.
- ↑Loeb, Jacques, and J. Northrop. “On the influence of food and temperature upon the duration of life.” The Journal of Biological hemistry 32, 103-121. October 1, 1917.
- ↑Austad, Steven N. “Life extension by dietary restriction in the bowl and doily spider, Frontinella pyramitela." Experimental gerontology 24.1 (1989): 83-92.
- ↑Comfort, Alex. “Effect of Delayed and Resumed Growth on the Longevity of a Fish (Lebistes reticulatus, Peters) in Captivity." Gerontology 8.2-3 (1963): 150-155.
- ↑McCay, CMw, Mary F. Crowell, and L. A. Maynard. “The effect of retarded growth upon the length of life span and upon the ultimate body size." Journal of Nutrition 10, no. 1 (1935): 63-79.
- ↑Goldberg, Emily L., Melissa J. Romero‐Aleshire, Kristin R. Renkema, Melissa S. Ventevogel, Wade M. Chew, Jennifer L. Uhrlaub, Megan J. Smithey et al. “Lifespan-extending caloric restriction or mTOR inhibition impair adaptive immunity of old mice by distinct mechanisms." Aging Cell 14, no. 1 (2015): 130-138.
- ↑“In a population of rhesus macaques maintained at the Wisconsin National Primate Research Center, moderate CR lowered the incidence of aging-related deaths. At the time point reported 50% of control fed animals survived compared with 80% survival of CR animals. Further, CR delayed the onset of age-associated pathologies. Specifically, CR reduced the incidence of diabetes, cancer, cardiovascular disease, and brain atrophy.” Colman, Ricki J., Rozalyn M. Anderson, Sterling C. Johnson, Erik K. Kastman, Kristopher J. Kosmatka, T. Mark Beasley, David B. Allison, et al. “Caloric restriction delays disease onset and mortality in rhesus monkeys.” Science (New York, N.Y.) 325, no. 5937 (July 10, 2009): 201–4. Abstract.
- ↑Mattison, Julie A., George S. Roth, T. Mark Beasley, Edward M. Tilmont, April H. Handy, Richard L. Herbert, Dan L. Longo, et al. “Impact of caloric restriction on health and survival in rhesus monkeys: the NIA study.” Nature 489, no. 7415 (September 13, 2012).
- ↑石神昭人「カロリー制限しても寿命は延びない」東京都健康長寿医療センター研究所. 老化制御研究チーム. ただし、石神は、2017年の『ネイチャー・コミュニケーションズ』の結論を受けて、「論争に一つの終止符が打たれた。約30年に及ぶカロリー制限の研究データは、人間にも置き換えることができそうだ」と述べたと報道されている。小川裕介「カロリー制限、やっぱり長寿に効果 論争に終止符か」『朝日新聞』2017年1月18日07時52分.
- ↑Mattison, Julie A., Ricki J. Colman, T. Mark Beasley, David B. Allison, Joseph W. Kemnitz, George S. Roth, Donald K. Ingram, Richard Weindruch, Rafael de Cabo, and Rozalyn M. Anderson. “Caloric restriction improves health and survival of rhesus monkeys.” Nature Communications 8 (January 17, 2017): 14063. Figure 6 (a) “Morbidity curves for monkeys at NIA and UW shown.” Licensed under CC-BY-SA. 引用者によるレイアウトの変更あり。
- ↑Mattison, Julie A., Ricki J. Colman, T. Mark Beasley, David B. Allison, Joseph W. Kemnitz, George S. Roth, Donald K. Ingram, Richard Weindruch, Rafael de Cabo, and Rozalyn M. Anderson. “Caloric restriction improves health and survival of rhesus monkeys.” Nature Communications 8 (January 17, 2017): 14063. Figure 2 (b) “Bodyweight data for monkeys at NIA and UW”. Licensed under CC-BY-SA.
- ↑Grove, K. L., et al. “A microarray analysis of sexual dimorphism of adipose tissues in high-fat-diet-induced obese mice." International Journal of Obesity 34.6 (2010): 989-1000.
- ↑飢餓を体験した被験者は、基礎代謝率が低下し、体温が低下し、呼吸と心拍数が低下した。一部の被験者は、血漿タンパク質のレベルが低下したために、四肢に浮腫を示した。この他、鬱病、ヒステリー症、羊膜炎症が有意に増加したということである。
- ↑Ravussin, Eric, et al. “A 2-Year Randomized Controlled Trial of Human Caloric Restriction: Feasibility and Effects on Predictors of Health Span and Longevity." The Journals of Gerontology Series A: Biological Sciences and Medical Sciences 70.9 (2015): 1097-1104.
- ↑Villareal, Dennis T., Luigi Fontana, Sai Krupa Das, Leanne Redman, Steven R. Smith, Edward Saltzman, Connie Bales et al. “Effect of Two-Year Caloric Restriction on Bone Metabolism and Bone Mineral Density in Non-Obese Younger Adults: A Randomized Clinical Trial." Journal of Bone and Mineral Research 31, no. 1 (2016): 40-51.
- ↑Romashkan, Sergei V., Sai Krupa Das, Dennis T. Villareal, Eric Ravussin, Leanne M. Redman, James Rochon, Manjushri Bhapkar, William E. Kraus, andCALERIEStudy Group. “Safety of two-year caloric restriction in non-obese healthy individuals." Oncotarget 7, no. 15 (2016): 19124.
- ↑Meydani, Simin N., Sai K. Das, Carl F. Pieper, Michael R. Lewis, Sam Klein, Vishwa D. Dixit, Alok K. Gupta, et al. “Long-term moderate calorie restriction inhibits inflammation without impairing cell-mediated immunity: a randomized controlled trial in non-obese humans.” Aging (Albany NY) 8, no. 7 (July 13, 2016): 1416–26.
- ↑ICAM-1(炎症性サイトカインとともに増える細胞間接着分子)は、対照群と比較して、実験群では一年後有意に減ったが、二年後には有意な差がなくなった。
- ↑Yang, Ling, et al. “Long-Term Calorie Restriction Enhances Cellular Quality-Control Processes in Human Skeletal Muscle." Cell reports 14.3 (2016): 422-428.
- ↑Dey, D. K., et al. “Body mass index, weight change and mortality in the elderly. A 15 y longitudinal population study of 70 y olds." European Journal of Clinical Nutrition 55.6 (2001): 482.
- ↑World Health Organization. “The International Classification of adult underweight, overweight and obesity according to BMI.” Global Database on Body Mass Index. 9 May 2009.
- ↑Sasazuki, Shizuka, Manami Inoue, Ichiro Tsuji, Yumi Sugawara, Akiko Tamakoshi, Keitaro Matsuo, Kenji Wakai, et al. “Body Mass Index and Mortality From All Causes and Major Causes in Japanese: Results of a Pooled Analysis of 7 Large-Scale Cohort Studies.” Journal of Epidemiology 21, no. 6 (November 5, 2011): 417–30.
- ↑Adams, K. F., M. F. Leitzmann, R. Ballard-Barbash, D. Albanes, T. B. Harris, A. Hollenbeck, and V. Kipnis. “Body Mass and Weight Change in Adults in Relation to Mortality Risk.” American Journal of Epidemiology 179, no. 2 (January 15, 2014): 135–44.
- ↑近藤 祥司.『老化はなぜ進むのか―遺伝子レベルで解明された巧妙なメカニズム』講談社 (2009/12/22). p.145.
- ↑Holliday, Robin. “Food, reproduction and L’ongevity: Is the extended lifespan of calorie-restricted animals an evolutionary adaptation?" Bioessays 10, no. 4 (1989): 125-127.
- ↑Kaeberlein, Matt, Mitch McVey, and Leonard Guarente. “The SIR2/3/4 complex and SIR2 alone promote longevity in Saccharomyces cerevisiae by two different mechanisms." Genes & Development 13, no. 19 (1999): 2570-2580.
- ↑Lin, Su-Ju, Pierre-Antoine Defossez, and Leonard Guarente. “Requirement of NAD and SIR2 for Life-Span Extension by Calorie Restriction in Saccharomyces cerevisiae." Science 289, no. 5487 (2000): 2126-2128.
- ↑Morselli, Eugenia, Maria Chiara Maiuri, Maria Markaki, Evgenia Megalou, Angela Pasparaki, Konstantinos Palikaras, Alfredo Criollo et al. “The life span-prolonging effect of Sirtuin-1 is mediated by autophagy." Autophagy 6, no. 1 (2010): 186-188.
- ↑Ghosh, Hiyaa Singhee, Michael McBurney, and Paul D. Robbins. “SIRT1 Negatively Regulates the Mammalian Target of Rapamycin.” PLoS ONE 5, no. 2 (February 15, 2010). ただし、腸幹細胞におけるmTORC1シグナルは、カロリー制限により逆に上昇する。これに関しては、Igarashi, Masaki, and Leonard Guarente. “mTORC1 and SIRT1 Cooperate to Foster Expansion of Gut Adult Stem Cells during Calorie Restriction." Cell 166, no. 2 (2016): 436-450. を参照されたい。栄養が欠乏するときは、腸の吸収効率を高めなければならないからだろう。
- ↑Sukumar, Deeptha, et al. “Areal and volumetric bone mineral density and geometry at two levels of protein intake during caloric restriction: A randomized, controlled trial." Journal of bone and mineral research 26.6 (2011): 1339-1348. ただし、間葉系幹細胞を用いた骨粗鬆症に関する研究で、SIRT1がPPAR-γを抑制することで、骨芽細胞の増加と脂肪細胞の減少を促す機序が報告されている。これに関しては、以下の論文を参照されたい。Bäckesjö, Carl‐Magnus, et al. “Activation of Sirt1 Decreases Adipocyte Formation During Osteoblast Differentiation of Mesenchymal Stem Cells." Journal of Bone and Mineral Research 21.7 (2006): 993-1002; Amat, Ramon, Anna Planavila, Shen Liang Chen, Roser Iglesias, Marta Giralt, and Francesc Villarroya. “SIRT1 Controls the Transcription of the Peroxisome Proliferator-activated Receptor-γ Co-activator-1α (PGC-1α) Gene in Skeletal Muscle through the PGC-1α Autoregulatory Loop and Interaction with MyoD." Journal of Biological Chemistry 284, no. 33 (2009): 21872-21880.
- ↑ヒトにおけるカロリー制限は、PI3K/AKT経路を、したがって、IGF-1/インスリン経路を阻害し、若年者に似た骨格筋の転写プロファイルの変化を誘導することが示されている。Mercken, Evi M., et al. “Calorie restriction in humans inhibits the PI3K/AKT pathway and induces a younger transcription profile." Aging cell 12.4 (2013): 645-651.
- ↑Surbey, Michele K. “Anorexia nervosa, amenorrhea, and adaptation." Ethology and Sociobiology 8 (1987): 47-61.
- ↑Cangemi, Roberto, Alberto J. Friedmann, John O. Holloszy, and Luigi Fontana. “Long-term effects of calorie restriction on serum sex-hormone concentrations in men." Aging cell 9, no. 2 (2010): 236-242.
- ↑Selesniemi, Kaisa, Ho‐Joon Lee, and Jonathan L. Tilly. “Moderate caloric restriction initiated in rodents during adulthood sustains function of the female reproductive axis into advanced chronological age." Aging cell 7, no. 5 (2008): 622-629.
- ↑Swindell, William R. “Dietary Restriction in Rats and Mice: A Meta-Analysis and Review of the Evidence for Genotype-Dependent Effects on Lifespan.” Ageing Research Reviews 11, no. 2 (April 1, 2012): 254–70.






















ディスカッション
コメント一覧
まだ、コメントがありません